संपर्क करना:एरोल झोउ (श्री)
दूरभाष: प्लस 86-551-65523315
मोबाइल/व्हाट्सएप: प्लस 86 17705606359
क्यूक्यू:196299583
स्काइप:lucytoday@hotmail.com
ईमेल:sales@homesunshinepharma.com
जोड़ना:1002, हुआनमाओ बिल्डिंग, नंबर 105, मेंगचेंग रोड, हेफ़ेई सिटी, 230061, चीन
दिसंबर 2017 में, Fosun Pharma ने Ardelyx से चीन (मुख्यभूमि चीन, हांगकांग और मकाऊ विशेष प्रशासनिक क्षेत्रों सहित) में टेनपैनोर का विशेष विकास और व्यावसायीकरण लाइसेंस प्राप्त किया। सितंबर 2019 में, Tenapanor टैबलेट IBS-C क्लिनिकल परीक्षण अनुप्रयोगों को स्वीकार किया गया था; दिसंबर 2019 में, टेनपैनोर टैबलेट हाइपरफॉस्फेटेमिया क्लिनिकल परीक्षण आवेदन स्वीकार किए गए थे।
IBS-C के उपचार में, टेनपैनोर आंतों के उपकला कोशिकाओं की ऊपरी सतह पर NHE3 को रोककर छोटी आंत और बृहदान्त्र द्वारा सोडियम के अवशोषण को कम करता है, जिससे आंतों के लुमेन में पानी के स्राव में वृद्धि होती है, जिससे आंतों में तेजी आती है। क्रमाकुंचन और मल को नरम और ढीला बनाना। आईबीएस-सी वाले मरीजों में मल त्याग में वृद्धि हुई है और पेट दर्द कम हो गया है। पशु मॉडल में, टेनपैनोर को आंत की अतिसंवेदनशीलता को कम करके और आंतों की पारगम्यता को कम करके पेट दर्द को कम करने के लिए भी दिखाया गया है। बृहदान्त्र अतिसंवेदनशीलता के एक चूहे के मॉडल में, टेनपैनोर ने आंत के हाइपरलेजेसिया (वीएचएल) को कम कर दिया और बृहदान्त्र संवेदी न्यूरॉन्स की उत्तेजना को सामान्य कर दिया।
संयुक्त राज्य अमेरिका में, सितंबर 2020 में, टेनपैनोर (व्यापार का नाम: इब्स्रेला, 50mg टैबलेट) को FDA द्वारा अनुमोदित किया गया था। IBS-C वाले वयस्क रोगियों के उपचार, मल त्याग में वृद्धि और पेट दर्द को कम करने के लिए दवा को दिन में दो बार मौखिक रूप से लिया जाता है। यह ध्यान दिया जाना चाहिए कि IBS-C के उपचार में, Ibsrela दवा लेबल के साथ एक ब्लैक बॉक्स चेतावनी होती है: यह इंगित करता है कि बाल रोगियों में गंभीर निर्जलीकरण का खतरा है। 6 वर्ष से कम उम्र के रोगियों में दवा का उपयोग करने के लिए मना किया गया है। युवा चूहों में, टेनपैनोर मृत्यु का कारण बन सकता है, संभवतः निर्जलीकरण के कारण। इब्सरेला का उपयोग 6 से 12 वर्ष से कम उम्र के रोगियों में नहीं किया जाना चाहिए। 18 वर्ष से कम आयु के बाल रोगियों में इब्स्रेला की सुरक्षा और प्रभावशीलता स्थापित नहीं की गई है।
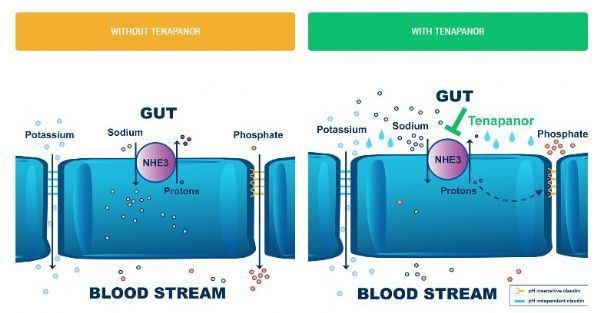
कार्रवाई का टेनपैनोर तंत्र
सीकेडी डायलिसिस रोगियों में हाइपरफोस्फेटेमिया के उपचार में, चूंकि NHE3 का कार्य प्रोटॉन (H+) का आदान-प्रदान करना और सोडियम (Na+) को अवशोषित करना है, टेनपैनोर आंतों के उपकला कोशिकाओं की ऊपरी सतह पर NHE3 को रोकता है। और इंट्रासेल्युलर प्रोटॉन (H+) को बढ़ाता है। प्रोटॉन (एच +) कोशिकाओं के बीच संबंधों को चुनिंदा रूप से कसते हैं, जिससे उपकला सेल कनेक्शन में संरचना परिवर्तन होता है, फॉस्फेट-विशिष्ट पारगम्यता को कम करता है, जिससे पैरासेलुलर मार्ग (पैरासेलुलर मार्ग, आहार फॉस्फेट अवशोषण के लिए मुख्य मार्ग) होता है। फॉस्फेट कम हो जाता है, जिससे सीरम फास्फोरस का स्तर कम हो जाता है। पैरासेलुलर मार्ग उस मार्ग को संदर्भित करता है जिसके माध्यम से पोषक तत्व और पानी आसन्न उपकला कोशिकाओं के बीच तंग जंक्शनों के माध्यम से अंतरकोशिकीय स्थान में प्रवेश करते हैं, और फिर रक्त में। क्लिनिकल और प्रीक्लिनिकल डेटा से पता चलता है कि टेनपैनोर NHE3 को रोकता है और मैक्रोमोलेक्यूल्स के अवशोषण मार्ग पर इसका कोई प्रभाव नहीं पड़ता है।
अर्डेलिक्स ने सीकेडी डायलिसिस के साथ वयस्क रोगियों में सीरम फास्फोरस को नियंत्रित करने में टेनपैनोर की प्रभावकारिता और सुरक्षा का मूल्यांकन करने के लिए 3 चरण 3 नैदानिक परीक्षण किए हैं: (1) 2 मोनोथेरेपी परीक्षण-अल्पकालिक मोनोथेरेपी चरण 3 ब्लॉक अध्ययन (एन=219, 12 सप्ताह ), दीर्घकालिक एकल-एजेंट चिकित्सा चरण ३ PHREEDOM अध्ययन (n=४२३, ५२ सप्ताह); (२) १ दोहरी तंत्र परीक्षण-चरण ३ एम्पलीफ अध्ययन (एन=२३५, ४ सप्ताह), टेनपैनोर संयोजन का मूल्यांकन फॉस्फेट बाइंडरों की दोहरी-तंत्र चिकित्सा की तुलना एकल-उपयोग फॉस्फेट बाइंडरों के साथ की जाती है।
सभी तीन चरण 3 परीक्षणों ने प्राथमिक और प्रमुख माध्यमिक समापन बिंदुओं को पूरा किया: टेनपैनोर, अल्पकालिक, दीर्घकालिक, और फॉस्फेट बाइंडरों के साथ संयोजन ने सीरम फास्फोरस के स्तर को काफी कम कर दिया। Ardelyx सामान्य फॉस्फोरस स्तर (2.5-4.5 मिलीग्राम / डीएल) तक पहुंचने के लिए अकेले टेनपैनोर की क्षमता का आकलन करने के लिए या सेवेलमर के संयोजन में एक सामान्य ओपन-लेबल एक्सटेंशन अध्ययन (एन=171) भी आयोजित कर रहा है।