संपर्क करना:एरोल झोउ (श्री)
दूरभाष: प्लस 86-551-65523315
मोबाइल/व्हाट्सएप: प्लस 86 17705606359
क्यूक्यू:196299583
स्काइप:lucytoday@hotmail.com
ईमेल:sales@homesunshinepharma.com
जोड़ना:1002, हुआनमाओ बिल्डिंग, नंबर 105, मेंगचेंग रोड, हेफ़ेई सिटी, 230061, चीन
गैलापागोस एनवी ने हाल ही में सोरायसिस के रोगियों के उपचार में टाइरोसिन किनसे 2 (TYK2) अवरोधक GLPG3667 के चरण 1b अध्ययन के सकारात्मक शीर्ष-पंक्ति परिणामों की घोषणा की। GLPG3667 की खोज गैलापागोस ने की थी और यह एक मालिकाना चयनात्मक TYK2 यौगिक है। एक यादृच्छिक, प्लेसबो-नियंत्रित, डबल-ब्लाइंड चरण 1 बी अध्ययन में, मध्यम से गंभीर पट्टिका सोरायसिस के निदान वाले 31 रोगियों का इलाज किया गया। अध्ययन में, रोगियों को कुल 4 सप्ताह के उपचार के लिए 1:1:1 के अनुपात में प्रतिदिन GLPG3667 (कम या उच्च खुराक) या प्लेसीबो लेने के लिए यादृच्छिक रूप से असाइन किया गया था। मुख्य उद्देश्य चौथे सप्ताह में GLPG3667 की सुरक्षा, सहनशीलता और नैदानिक गतिविधि के संकेतों का मूल्यांकन करना है।
परिणामों से पता चला कि चरण 1बी परीक्षण में GLPG3667 को अच्छी तरह से सहन किया गया था। कम खुराक वाले समूह के एक मरीज ने सोरायसिस के बिगड़ने के कारण एक दिन के लिए इलाज बंद कर दिया। उपचार से संबंधित अधिकांश प्रतिकूल घटनाएं (एई) प्रकृति में हल्की और अस्थायी होती हैं। इस 4 सप्ताह के अध्ययन में, कोई मौत या गंभीर प्रतिकूल घटनाएं नहीं हुईं।
सप्ताह 4 में, GLPG3667 उच्च-खुराक समूह में 10 में से 4 रोगियों ने PASI50 प्रतिक्रिया प्राप्त की (सोरायसिस क्षेत्र और गंभीरता सूचकांक [PASI] बेसलाइन से कम से कम 50% सुधार हुआ) प्रतिक्रिया, और प्लेसबो समूह में 10 में से 1 रोगी एक PASI50 प्रतिक्रिया हासिल की। PASI50 ने जवाब दिया। हालाँकि, GLPG3667 कम खुराक वाले समूह के किसी भी मरीज ने PASI50 प्रतिक्रिया हासिल नहीं की। बेसलाइन स्तरों की तुलना में GLPG3667 उच्च-खुराक समूह में 4 उत्तरदाताओं के PASI स्कोर में क्रमशः 52%, 65%, 74% और 81% का सुधार हुआ, जबकि प्लेसीबो समूह में 1 उत्तरदाता में बेसलाइन की तुलना में 52% सुधार हुआ। . चौथे सप्ताह में, प्लेसबो की तुलना में, उच्च खुराक वाले GLPG3667 ने अन्य समापन बिंदुओं (शरीर की सतह के प्रभावित क्षेत्र, डॉक्टर और रोगी के समग्र मूल्यांकन सहित) के लिए सकारात्मक प्रभावकारिता संकेत देखे।
गैलापागोस के मुख्य चिकित्सा अधिकारी डॉ. वालिद अबी साब ने कहा: [जीजी] उद्धरण; हम 4 सप्ताह के लिए सोरायसिस के रोगियों में जीएलपीजी 3667 के साथ देखे गए प्रभावकारिता संकेतों और सुरक्षा से संतुष्ट हैं। इन परिणामों के आधार पर, हम अगले साल सोरायसिस ग्लोबल फेज 2बी प्रोजेक्ट लॉन्च करने की योजना बना रहे हैं। हमारे चयनात्मक मौखिक TYK2 अवरोधक GLPG3667 परियोजना के विकास के हिस्से के रूप में, परियोजना का उद्देश्य भड़काऊ संकेतों की एक विस्तृत श्रृंखला के लिए GPLG3667 का मूल्यांकन करना है। [जीजी] उद्धरण;
जर्मनी के लुबेक विश्वविद्यालय में व्यापक सूजन चिकित्सा केंद्र में मेडिसिन के प्रोफेसर डॉ। डायमंत थासी ने कहा: "केवल 4 सप्ताह के उपचार के बाद PASI50 प्रतिक्रिया स्कोर और अन्य प्रभावकारिता डेटा, देखी गई सुरक्षा के साथ संयुक्त, बहुत मददगार हैं यौगिक को बड़े पैमाने पर आगे बढ़ाने में। सोरायसिस परीक्षण। सोरायसिस रोगियों को अभी भी अधिक उपचार विकल्पों की आवश्यकता है, विशेष रूप से मौखिक चिकित्सा। [जीजी] उद्धरण;
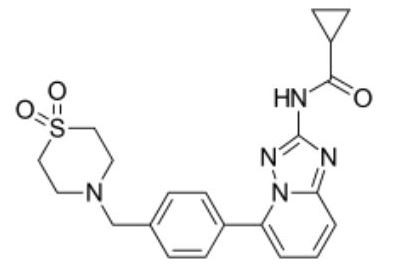
जेसेलेका-फिल्गोटिनिबरासायनिक संरचना
गैलापागोस कार्रवाई के नए तंत्र के साथ छोटी अणु दवाओं की खोज और विकास के लिए प्रतिबद्ध है, जिनमें से कुछ ने अच्छी प्रभावकारिता दिखाई है। वर्तमान में, कंपनी गिलियड साइंसेज के साथ एक मौखिक विरोधी भड़काऊ दवा Jyseleca (filgotinib) विकसित करने के लिए काम कर रही है।
फिल्गोटिनिबगैलापागोस द्वारा खोजा और विकसित किया गया एक अत्यधिक चयनात्मक JAK1 अवरोधक है। दिसंबर 2015 के अंत में, गिलियड ने गैलापागोस के साथ कुल मिलाकर 2 बिलियन अमेरिकी डॉलर तक का समझौता किया, ताकि विश्व स्तर पर फिल्गोटिनिब को संयुक्त रूप से विकसित और व्यावसायीकरण किया जा सके। हालांकि, अमेरिकी विनियमन में बड़े झटके के कारण, दोनों पक्षों ने दिसंबर 2020 में फिल्गोटिनिब के व्यावसायीकरण और विकास समझौते को संशोधित किया। गैलापागोस यूरोप में फिल्गोटिनिब के व्यावसायीकरण के लिए जिम्मेदार होगा (संक्रमण अवधि 2021 के अंत में पूरी होने की उम्मीद है)। ), जबकि गिलियड यूरोप के बाहर फिल्गोटिनिब के लिए जिम्मेदार बना रहेगा, जिसमें जापान भी शामिल है (जहां गिलियड संयुक्त रूप से इसाई के साथ फिल्गोटिनिब की बिक्री करेगा)।
फिल्गोटिनिबविभिन्न प्रकार की सूजन संबंधी बीमारियों के इलाज के लिए विकसित किया जा रहा है, जिनमें से चरण 3 के अध्ययनों में रुमेटीइड गठिया, क्रोहन [जीजी] #39; रोग, और अल्सरेटिव कोलाइटिस का उपचार शामिल है।
Jyseleca को यूरोपीय संघ, यूनाइटेड किंगडम और जापान में मध्यम से गंभीर संधिशोथ (RA) वाले वयस्क रोगियों के इलाज के लिए विपणन के लिए अनुमोदित किया गया है, जिनके पास एक या अधिक रोग-संशोधित एंटी-रूमेटिक दवाओं के लिए अपर्याप्त प्रतिक्रिया या असहिष्णुता है ( डीएमएआरडी)। दवा के संदर्भ में, Jyseleca का उपयोग मोनोथेरेपी के रूप में या मेथोट्रेक्सेट (MTX) के संयोजन में किया जा सकता है।
वर्तमान में, अल्सरेटिव कोलाइटिस (UC) के उपचार के लिए नए संकेतों के लिए Jyseleca' का आवेदन भी यूरोपीय संघ, यूनाइटेड किंगडम और जापान में नियामक समीक्षा के दौर से गुजर रहा है। विशिष्ट अनुप्रयोग है: अपर्याप्त प्रतिक्रिया के उपचार के लिए, प्रतिक्रिया करने में विफलता, या पारंपरिक उपचारों या जैविक एजेंटों के प्रति असहिष्णुता मध्यम से गंभीर सक्रिय अल्सरेटिव कोलाइटिस (यूसी) वाले वयस्क रोगी। यह ध्यान देने योग्य है कि यूएस एफडीए ने सुरक्षा कारणों से जेसेलेका के लिए किसी भी संकेत को मंजूरी नहीं दी है।